코로나19에 대한 먹는 치료제 소식이 전해진 가운데 치료약이 승인되더라도 백신은 필요하다는 주장이 나왔다.
파우치 미국 국립알레르기·전염병연구소(NIAID) 소장은 3일(현지시간) ABC방송에 출연해 '치료제가 승인되면 백신이 불필요한가'라는 질문에 "분명히 아니다. '이제 여러분은 약을 갖고 있다'고 말하는 것은 너무나 잘못된 얘기"라고 했다.
앞서 미 제약사 머크앤컴퍼니(MSD)는 지난 1일 경구용 항바이러스 치료제 '몰누피라비르'가 경증 또는 중간 증세의 감염 5일 이내 코로나19 환자 775명을 상대로 한 3차 임상시험에서 입원 가능성을 50%가량 낮췄다며 코로나 치료에 효과적이라고 발표한 바 있다.
MSD는 이 약 복용자 가운데 7.3%만이 29일 이내에 코로나로 병원에 입원했지만, 위약(가짜 약·플라시보) 복용자 중 14.1%가 입원하거나 사망했다고 밝혔다. 약 복용자 누구도 사망하지 않았지만 위약 복용자는 8명이 사망했다고도 했다.
파우치 소장은 "잊지 말라. 병원에 가지 않고 죽지 않는 가장 쉬운 방법은 감염되지 않는 것"이라며 "'우리가 약을 가지고 있으니 백신을 안 맞아도 된다'는 그런 생각은 전혀 말이 안 된다"고 말했다.
그는 또 "많은 사망자가 백신을 맞았더라면 죽음을 피할 수 있었을 것"이라면서 "병원에 입원하고 사망하는 사람들을 보면, 백신 미접종자가 압도적"이라고 했다.
파우치 소장은 지난 1일 MSD의 치료제 시험 결과 소식이 전해지자 식품의약국(FDA)이 최대한 빨리 긴급 사용승인을 심사할 것이라고 말한 바 있다.
다른 전문가들도 머크 알약이 백신을 대체하는 것이 아니라 보완하는 역할이라고 당부하고 있다.
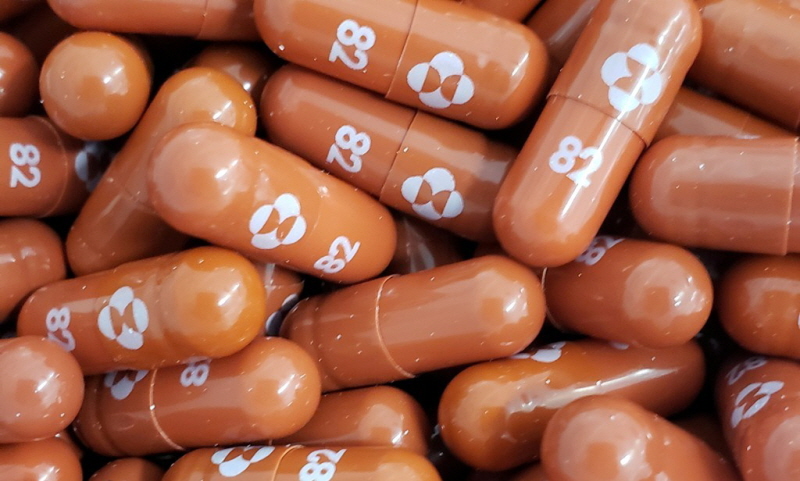
1일 로이터·AFP통신 등 주요 외신에 따르면 머크와 리지백 바이오테라퓨틱스는 가벼운 또는 중간 정도의 증세를 보이는 감염 5일 이내의 코로나19 환자 775명을 대상으로 '몰누피라비르'의 3상 임상시험을 진행했다.
임상시험 참가자 절반은 물누피라비르 알약을, 나머지 절반은 플라시보(가짜 약)를 각각 5일간 복용하는 방식으로 진행됐다. 그 결과 29일 뒤 몰누피라비르를 복용한 환자 가운데 7.3%만이 병원에 입원했고 사망자는 나오지 않았다.
플라시보 복용군의 입원률이 14.1%를 기록한 것과 비교하면 이 알약이 코로나19 환자의 입원 가능성을 50% 가량 낮춰준 셈이라고 회사 측은 설명했다. 플라시보를 복용한 임상시험 참가자 중에서는 8명이 사망했다.
머크는 신속히 미 식품의약국(FDA)에 이 알약의 긴급사용 승인(EUA)을 신청하고, 다른 국가에서도 신청을 서두르겠다고 밝혔다.
FDA가 허가하면 몰누피라비르는 첫 코로나19 알약 치료제가 된다. 미 제약사 화이자와 스위스 제약사 로슈도 코로나19 치료를 위한 경구용 항바이러스제를 개발 중이지만 속도가 늦어지고 있다.
몰누피라비르는 코로나19 바이러스의 유전암호 오류를 유도하는 방식으로 작용해 델타 변이를 포함한 모든 변이에 효과가 있다는 자체 연구 결과도 나왔다. 다만 인간 세포에서 유전적 변화를 유도하지는 않는다고 회사 측은 설명했다.
머크는 올해 말까지 1000만 명에게 투약할 수 있는 물량을 생산하고, 내년에는 생산량을 더 늘릴 수 있을 것으로 보고 있다.
미 정부에는 170만 명 치료분을 공급하기로 계약했으며, 다른 나라 정부들과도 비슷한 계약을 합의한 상태라고 회사 측은 전했다. 약값은 각국의 소득 수준을 고려해 다르게 책정할 방침이다. 미국에는 1명 치료분을 700달러(약 83만원)에 팔기로 했다.